La lucha contra las células de la sangre dobladas
octubre de 2020
Artículo destacado
La lucha contra las células de la sangre dobladas
Progresos de la enfermedad de células falciformes

Con cada latido del corazón, la sangre transporta oxígeno desde los pulmones a todo el cuerpo. Este proceso de soporte vital ocurre de forma automática, tanto si está despierto o dormido.
Sin embargo, para las personas con la enfermedad de células falciformes, este proceso suele salir mal. Las personas con esta enfermedad tienen un tipo anormal de hemoglobina, la molécula que transporta oxígeno en los glóbulos rojos.
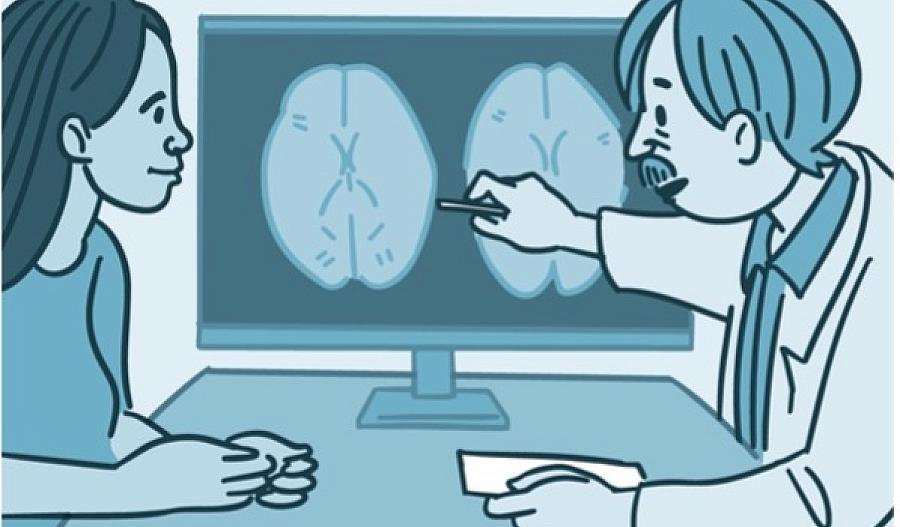
Normalmente, los glóbulos rojos son flexibles y tienen forma de disco, sin embargo, la hemoglobina en las personas con la enfermedad de células falciformes produce glóbulos rojos de forma anormal. Por lo general, tienen forma de media luna (o forma de hoz).
Estas células dobladas e inflexibles pueden adherirse a las paredes de los vasos sanguíneos. Las acumulaciones resultantes ralentizan o detienen el flujo de sangre. Esto puede provocar dolor y daño de los órganos.
“La anemia de células falciformes puede potencialmente bloquear el suministro de sangre a cualquier órgano del cuerpo”, explica el Dr. Swee Lay Thein, experto en trastornos de la sangre de los Institutos Nacionales de la Salud (NIH).
La mayoría de las personas con la enfermedad de células falciformes solían morir antes de llegar a la edad adulta. Sin embargo, con los tratamientos modernos, las personas en los EE. UU. ahora viven hasta los 40, 50 o incluso 60 años. Además, los investigadores trabajan en terapias avanzadas, como reparar el gen roto que causa la enfermedad.
"Creo que el tratamiento será muy diferente en los próximos 20 años", dice la Dra. Allison King, experta en la enfermedad de células falciformes en niños en la Universidad de Washington en St. Louis.
Un gen, muchos síntomas
Los cambios en un solo gen pueden causar la enfermedad de células falciformes. Sin embargo, todo el mundo tiene dos copias del gen. Se hereda una copia de cada padre. Más de dos millones de personas en los EE. UU. tienen una copia anormal, llamada rasgo de células falciformes. Por lo general, no presentan ningún síntoma. Sin embargo, si hereda dos copias, el resultado es la enfermedad de células falciformes.
Alrededor de 100,000 personas en los EE. UU. viven con la enfermedad de células falciformes. La mayoría son afroamericanos. Sin embargo, a todos los bebés que nacen en los EE. UU. se les hace una prueba para detectar la enfermedad de células falciformes al nacer. Esto ayuda a los médicos a comenzar el tratamiento lo antes posible.
Los niños no suelen mostrar síntomas hasta que tienen entre seis y doce meses, explica Thein. Los glóbulos rojos de los bebés tienen un tipo diferente de hemoglobina, llamada hemoglobina fetal. A medida que crecen, el cuerpo pasa a producir hemoglobina adulta. Entonces, comienza el ciclo de la enfermedad de células falciforme.
Un glóbulo rojo normal vive entre tres y cuatro meses. Sin embargo, en las personas con la enfermedad de células falciformes, las células suelen vivir solo de dos a tres semanas. Esto provoca anemia, una afección en la cual la sangre tiene una cantidad baja de glóbulos rojos o hemoglobina. La anemia reduce el oxígeno en el cuerpo, lo que puede causar fatiga, mareos y dolores de cabeza.
El dolor es otro síntoma común. Puede ser tan grave que las personas terminan en el hospital. Estos episodios de dolor se llaman "crisis de células falciformes".
“La vida de las personas se ve alterada por estos episodios”, dice Thein. “Para los niños, eso significa faltar a la escuela. Los adultos pueden perder mucho trabajo".
El bloqueo del flujo sanguíneo al cerebro puede causar derrames cerebrales, incluso en niños. Los derrames cerebrales y las obstrucciones en los vasos sanguíneos de los pulmones son algunas de las complicaciones más peligrosas de la enfermedad, dice Thein.
Nuevas opciones de medicamentos
El tratamiento más común para la enfermedad de células falciformes es un medicamento llamado hidroxiurea. Este medicamento persuade al cuerpo adulto para que produzca hemoglobina fetal. Esto aumenta la cantidad de glóbulos rojos funcionales.
La hidroxiurea no funciona para todos. Sin embargo, se han aprobado tres nuevos tratamientos en los últimos años. Algunos de los medicamentos más nuevos evitan que las células falciformes se adhieran a los vasos sanguíneos.
En la actualidad, el equipo de Thein prueba un medicamento para evitar que las células de la sangre se doblen en primer lugar. “Eso sería lo más efectivo — para detener el proceso de formación de células falciformes —”, explica.
Aunque los medicamentos ayudan a muchas personas, tomarlos a diario puede ser difícil, explica King. Los niveles bajos de oxígeno en el cerebro en personas con la enfermedad de células falciformes pueden afectar la memoria. En la actualidad, King y sus colegas prueban formas de utilizar la tecnología, como las aplicaciones de teléfonos inteligentes, para ayudar a las personas a tomar sus medicamentos según lo recetado.
Algunas personas con la enfermedad de células falciformes pueden necesitar transfusiones de sangre periódicas o de emergencia, en las que reciben sangre donada.
Arreglar las células de la sangre
En la actualidad, la única cura para la enfermedad de células falciformes es un trasplante de médula ósea. La médula ósea es el tejido esponjoso que contiene las células madre que dan origen a las células de la sangre.
En un trasplante de médula ósea, se destruyen primero las células madre de la médula ósea del paciente que producen células de la sangre. Luego, las células madre de un donante sin la enfermedad de células falciformes se transfieren al paciente. Estas nuevas células madre producirán células de la sangre que no sean falciformes.
El procedimiento es riesgoso. Se considera muy peligroso para los adultos. Sin embargo, el problema principal, explica el Dr. Matthew Hsieh, investigador de trasplantes de los NIH; es que la mayoría de los niños no tienen un donante compatible. Si ciertas proteínas en las células del donante son diferentes a las del niño, el trasplante puede fallar.
Hsieh y otros han desarrollado nuevos métodos para trasplantar la médula ósea de personas que no son totalmente compatibles. También desarrollan formas de preparar la médula ósea para un trasplante que podría hacer que el procedimiento sea más seguro para los adultos.
En la actualidad, los investigadores también prueban un enfoque llamado terapia genética. En la terapia genética, se recolectan las propias células madre del paciente. Luego, se modifican en el laboratorio para corregir un gen. Por último, se regresan las células al paciente.
Un estudio reciente de terapia genética de los NIH agregó con éxito una copia funcional del gen de la hemoglobina a las células madre. Otro estudio analizará si las células adultas se pueden alterar para producir hemoglobina fetal.
Si vive con la enfermedad de células falciformes, hable con su proveedor de atención médica para desarrollar un plan de atención adecuado para usted. Mantener un estilo de vida saludable puede ayudarlo a prevenir o controlar algunas de sus complicaciones (vea el recuadro de Decisiones inteligentes para obtener consejos).
Si está interesado en participar en un estudio clínico, llame al 1-800-411-1222 o visite https://salud.nih.gov/investigacion-clinica/como-encontrar-un-estudio-clinico.
Elecciones sabias
Consejos para vivir con la enfermedad de células falciformes
- Consulte con su médico con regularidad. La mayoría de las personas con la enfermedad de células falciformes deben consultar a su médico cada 3 a 12 meses.
- Obtenga las vacunas recomendadas. Las personas con la enfermedad de células falciformes tienen un mayor riesgo de infección. Obtenga más información de los CDC: https://www.cdc.gov/spanish/inmunizacion/index.html.
- Adopte un estilo de vida saludable. Dormir lo suficiente, comer sano y evitar el alcohol y el tabaco pueden hacer que se sienta mejor y reducir el dolor.
- Controle el dolor. Trabaje con un especialista en dolor para elaborar un plan de tratamiento individual.
- Conozca y evite los factores desencadenantes. Muchas cosas pueden provocar el dolor. Las más comunes incluyen agotamiento y deshidratación.
Enlaces
- Preguntas y respuestas: la Dra. Allison King habla sobre la enfermedad de células falciformes y el aprendizaje
- Un trasplante revierte la anemia falciforme
- Anemia de células falciformes
- Enfermedad de células falciformes: consejos para una vida saludable
- Trasplante de médula ósea
- ¿Sabe reconocer un ataque cardíaco o un ACV?
- Conozca las señales súbitas de un ataque cerebral
Referencias
- Recent Advances in the Treatment of Sickle Cell Disease. Salinas Cisneros G, Thein SL. Front Physiol. 2020 May 20;11:435. doi: 10.3389/fphys.2020.00435. eCollection 2020. PMID:32508672.
- Optimal disease management and health monitoring in adults with sickle cell disease. Howard J, Thein SL. Hematology Am Soc Hematol Educ Program. 2019 Dec 6;2019(1):505-512. doi: 10.1182/hematology.2019000055. PMID: 31808832.
- Interactions of an Anti-Sickling Drug with Hemoglobin in Red Blood Cells from a Patient with Sickle Cell Anemia. Strader MB, Liang H, Meng F, Harper J, Ostrowski DA, Henry ER, Shet AS, Eaton WA, Thein SL, Alayash AI. Bioconjug Chem. 2019 Mar 20;30(3):568-571. doi: 10.1021/acs.bioconjchem.9b00130. Epub 2019 Feb 28. PMID: 30794381.
- Alternative Donor/Unrelated Donor Transplants for the β-Thalassemia and Sickle Cell Disease. Fitzhugh CD, Abraham A, Hsieh MM. Adv Exp Med Biol. 2017;1013:123-153. doi: 10.1007/978-1-4939-7299-9_5. PMID: 29127679.
- Curative therapies: Allogeneic hematopoietic cell transplantation from matched related donors using myeloablative, reduced intensity, and nonmyeloablative conditioning in sickle cell disease. Guilcher GMT, Truong TH, Saraf SL, Joseph JJ, Rondelli D, Hsieh MM. Semin Hematol. 2018 Apr;55(2):87-93. doi: 10.1053/j.seminhematol.2018.04.011. Epub 2018 Apr 25. PMID: 29958564.
- Increasing Educational Attainment in Adolescents with Sickle Cell Disease. Harris KM, Dadekian JN, Abel RA, Jones B, Housten A, Ddamulira B, Chadwick-Mansker K, King AA. Soc Work Public Health. 2019;34(6):468-482. doi: 10.1080/19371918.2019.1629142. Epub 2019 Jun 30. PMID: 31258020.